Très récemment, les nanobulles de gaz en solution dans l’eau ont fait l’objet d’une grande attention. Différents domaines de recherche sont impliqués en raison d’effets spectaculaires. Les nanobulles peuvent ainsi activer la croissance des huîtres. Elles autorisent la symbiose entre eau douce et eau salée pour les poissons dans le même aquarium. La préservation du nerf vague chez les rats semble nécessiter leur présence. Enfin, elles peuvent réagir très rapidement avec les hydrates de méthane. Ceci est d’autant plus surprenant que les nanobulles sont censées être thermodynamiquement instables en solutions aqueuses.
Équation de Young-Laplace et nanobulles
En effet, à pression atmosphérique la tension superficielle de l’interface air/eau est de γ ≈ 72 mN·m-1. Or, la pression interne au sein d’une nanobulle est gouvernée par l’équation de Young-Laplace p = 2×γ/r où r est le rayon de la nanobulle. On sait aujourd’hui que les nanobulles se forment dès que l’eau devient sursaturée en gaz. La figure qui illustre cette chronique montre des nanobulles de diazote, générées au moyen d’un dispositif spécial. Leur concentration est de 1,9·1019 nanobulles par litre d’eau. Elles sont observées par microscopie électronique à balayage sur des répliques gelées de ces solutions.
On trouve ainsi un rayon de 50 nanomètres pour la plupart de ses nanobulles. Ceci signifie qu’elles doivent avoir une pression interne proche 3 MPa. Or, cette pression interne est supérieure à celle de l’eau environnante (0,1 MPa). On devrait observer une diffusion du gaz depuis la bulle vers la solution. Les lois classiques de la diffusion prévoient ainsi une durée de vie de l’ordre de 1 microseconde pour une nanobulle en solution. Or, il n’en est rien et ces nanobulles peuvent avoir des durées de vie supérieures à deux semaines, ce qui est évidemment très surprenant.
Spectroscopie Raman et nanobulles
Des mesures par spectroscopie Raman réalisées sur ces nanobulles montrent que le diazote N2 est bien présent sous forme gazeuse dans ces solutions. On sait aussi qu’elles ne trouvent pas sous forme moléculaire solvatée par l’eau. Car, ceci provoquerait une légère diminution de 3 cm-1 de la fréquence de vibration N≡N par rapport au gaz (voir figure ci-dessous à droite) :
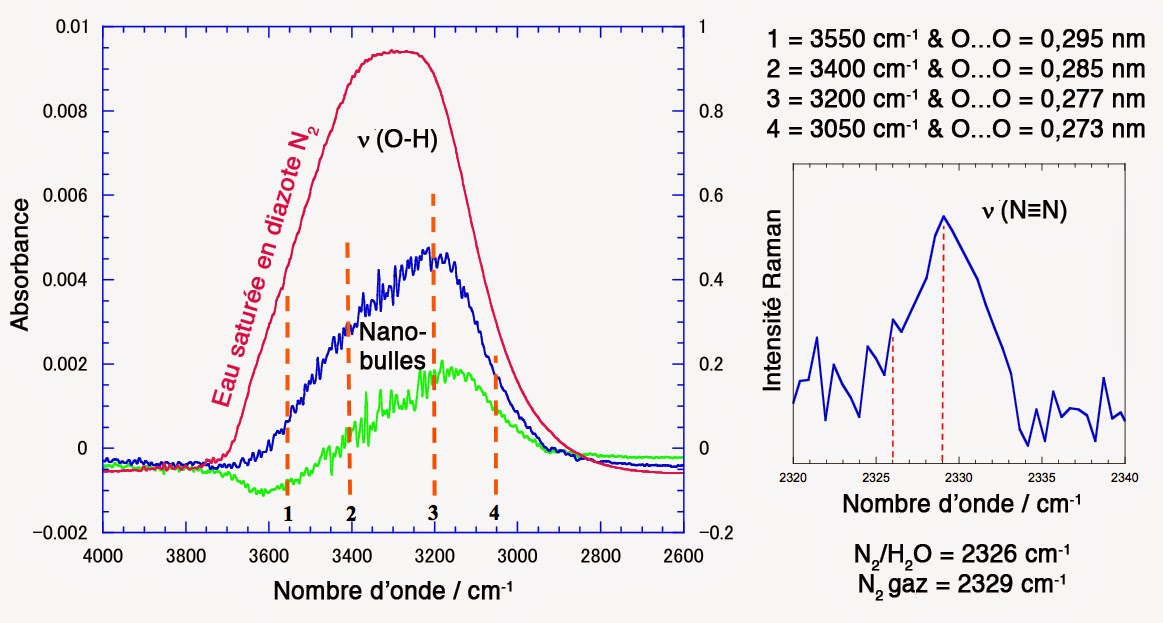
L’analyse du spectre infrarouge de ces nanobulles en solution (figure ci-dessus à gauche) révèle l’existence de liaisons hydrogène relativement fortes entre les molécules d’eau. Ces liaisons sont très similaires à celles que l’on trouve dans la glace ou dans les hydrates de méthane cristallisés. De plus, on constate que la pression interne de ces nanobulles est proche de 6 MPa. Cette valeur est deux fois supérieure à la valeur prévue par l’équation de Laplace compte tenu de leur rayon de 50 nm. Il existe donc une force mystérieuse qui empêche le gaz de diffuser à travers la frontière de ces nanobulles. Cela, malgré la très grande pression favorisant une telle diffusion vers la solution.
Stabilité des nanobulles
L’idée générale pour expliquer cette stabilité est qu’il y a accumulation de substances dissoutes à l’interface liquide-gaz. En effet, l’adsorption de manière dense de substances tensioactives à une interface induit de manière générale une barrière à la diffusion des gaz. Cet état de fait est exploité pour éviter l’évaporation dans les réservoirs. Il permet également de stabiliser les nanobulles en volume pour des agents de contraste. On peut donc imaginer qu’une dense couche de matière tensioactive à l’interface liquide-gaz d’une nanobulle aurait pour conséquence d’inhiber très fortement la diffusion du gaz piégé à l’intérieur de la nanobulle.
Une autre explication serait que la stabilité surprenante des nanobulles soit liée à la structuration de l’eau en domaines de cohérence. En effet, les solutés comme les bulles de gaz ne pouvant pénétrer à l’intérieur d’un domaine de cohérence. Ces derniers sont donc obligés de s’accumuler dans l’eau incohérente remplissant les interstices générés par les domaines de cohérence. Piégées dans un réseau inextricable de domaines de cohérence, la coalescence des nanobulles ne pourraient plus avoir lieu. En outre, les molécules de gaz qu’elles contiennent seraient contraintes de revenir dans la nanobulle après en être sorti. Ceci, suite à leur réflexion sur les parois infranchissables que représentent les domaines de cohérence.
Références
[1] K. Ohgaki, N. Q. Khanh, Y. Joden, A.Tsuji, T. Nakagawa T., «Physicochemical approach to nanobubble solutions», Chem. Eng. Sci., 65 (2010) 1296-1300.
[2] W. A. Ducker, «Contact Angle and Stability of Interfacial Nanobubbles», Langmuir, 25 (2009) 8907-8910.



Leave a Reply